3.1 EL BALANCE DE MATERIALES
El balance de materiales (también conocido como balance de masa), es un método utilizado para estimar las emisiones de algunas categorías de fuentes, en donde se conoce el volumen y la composición química de los insumos o materias primas utilizadas. El método de balance de materiales puede usarse en los casos en que no hay datos disponibles de muestreos en la fuente o factores de emisión aplicables.
El uso de un balance de materiales implica el análisis de un proceso para determinar si las emisiones pueden ser estimadas conociendo únicamente los parámetros específicos de operación y la composición de los materiales. Si bien el balance de materiales es una herramienta valiosa para estimar las emisiones de muchas fuentes, su aplicación requiere que se conozca cierta información sobre el material estudiado en cada punto a lo largo del proceso. El uso del balance de materiales es adecuado en los casos en que pueden conocerse los componentes del proceso.
Por medio del balance de materiales podemos evaluar la eficiencia de un proceso y calcular emisiones contaminantes al hacer una comparación entre las cantidades que entran y salen del mismo. Por ejemplo, si sabemos que en un proceso utilizamos un litro de thinner y en el producto resultante solamente encontramos 100ml, podemos asumir que los 900ml restantes se vaporizaron convirtiéndose en emisiones de las sustancias que lo componen.
3.1.1 Emisión de COVs (Compuestos Orgánicos Volátiles)
De hecho, para algunas fuentes, un balance de materiales es el único método práctico para estimar las emisiones con exactitud. Por ejemplo, en muchos casos, el muestreo en la fuente de emisiones de COVs, intermitentes o fugitivas puede ser muy difícil y costoso, por lo que es recomendable aplicar técnicas de estimación de emisiones a partir del balance de materiales.
Para obtener las emisiones de COVs de las fuentes puntuales y de área, por ejemplo, se usa por lo general un balance de materiales para estimar las emisiones por evaporación de solventes. Esta técnica es aplicable de igual manera a las fuentes puntuales y a las fuentes de área. En las fuentes puntuales se puede usar a nivel de dispositivo o de planta, mientras que en el caso de las fuentes de área el balance de materiales puede aplicarse a nivel regional o nacional.
El método más simple de balance de materiales es suponer que todo el solvente consumido por un proceso se evapora durante éste. Por ejemplo, es razonable suponer que durante muchas operaciones de pintura de superficies todo el solvente en la pintura se evapora a la atmósfera durante el proceso de secado. En tales casos, las emisiones simplemente son iguales a la cantidad de solvente aplicado en la pintura (y en los adelgazadores añadidos) como una función del tiempo. Otro ejemplo similar es el uso de solventes para lavado de ropa en seco, tal como se realiza en las tintorerías. Para estimar las emisiones de este tipo de procesos, sólo se requiere conocer la cantidad de solvente adquirido en cada tintorería durante el intervalo de tiempo de interés, porque se supone que las emisiones son iguales a la cantidad de solvente comprado.
En procesos donde se maneja una cantidad semifija de solvente, donde el solvente que se gasta es reemplazado cada determinado periodo o cada vez que es necesario, puede suponerse que el solvente gastado es equivalente a las emisiones.
La suposición de que el solvente de reemplazo es igual a las emisiones por evaporación también es útil en algunas situaciones más complicadas. Por ejemplo, si se emplea un equipo de control de emisiones no destructivo como un condensador o un absorbedor, esta suposición es válida en la medida que el solvente capturado sea regresado al proceso. De manera similar, esta suposición será aplicable si en la planta se practica la recuperación de solvente residual ya sea por destilación o por reducción o secado. Ambas prácticas reducen los requerimientos de solvente de reemplazo en el proceso y, por lo tanto, la cantidad de solvente que se convierte en emisiones fugitivas y que se pierde hacia la atmósfera.
Existen pruebas que proporcionan información sobre balance de materiales y determinaciones gravimétricas para varios procesos industriales, publicados por la American Society for Testing and Materials (ASTM) (Sociedad Americana para Pruebas y Materiales). En general, el uso de un balance de masa o de materiales para determinar las emisiones totales de un proceso es sencillo y costeable.
Los COVs totales emitidos de un proceso de mezclado de pintura por lotes, por ejemplo, se calcularía como se muestra a continuación (de acuerdo con el Método D 2369, de la ASTM):
COVent (lb/gal) – COVpm (lb/gal) = COVe (lb/gal) (3.1)
donde:
ent = que entra
pm = pintura mezclada
e = emitidos
Asimismo, el análisis del combustible puede usarse para predecir las emisiones de procesos de combustión, con base en la aplicación de las leyes de conservación de la materia. La presencia de ciertos elementos en los combustibles puede usarse para predecir su presencia en las corrientes de emisión.
Esto incluye elementos tóxicos tales como los metales que se encuentran en el carbón, así como el azufre que puede ser convertido en otros compuestos durante el proceso de combustión.
La ecuación básica que se usa en los cálculos de emisiones a partir del análisis del combustible es:

donde:
E = emisiones del contaminante
Qcomb. = Consumo de combustible, flujo másico (p.ej., kg/hr)
CCC = Concentración del contaminante en el combustible
MWce = Peso molecular del contaminante emitido (lb/lb-mol)
MWcc = Peso molecular del contaminante en el combustible (lb/lb-mol)
Por ejemplo, las emisiones de SO2 como producto de la quema de combustóleo pueden calcularse basándose en su contenido de azufre. De esta manera, se supone una conversión completa del azufre a SO2. Por lo tanto, por cada libra de azufre (PM=32 g) quemado se emiten dos libras de SO2 (PM= 64g).
Calcular las emisiones de SOx por hora (reportado como SO2) de una máquina de combustión interna que quema diesel, con base en los datos del análisis del combustible (el contenido de azufre). El consumo estimado de combustible es de 150 litros/hr. La densidad del diesel es de 0.85kg/litro (7.1 lb/gal). El contenido de azufre en el diesel es 0.05% en masa.
Consumo de combustible
Qcomb. = 150 litros/hr x 0.85 kg/litro
= 127.5 kg/hr
Concentración del contaminante en el combustible
CS = 0.05/100
= 0.0005
Contaminate emitido: SO2
Peso molecular del contaminante emitido
MWce = Peso molecular del SO2 = 64 lb/lb-mol
Peso molecular del contaminante en el combustible
MWcc = Peso molecular del S = 32 lb/lb-mol
Luego reemplazando en la Ecuación (3.2)
ESO2 = 127.5 x 0.0005 x (64/32)
= 0.13 kg/hr
En el ejemplo anterior el balance de materiales se simplifica porque se supone que todo el material que se está balanceando es emitido a la atmósfera. Sin embargo, existen situaciones en las que esta suposición no siempre es razonable. Por ejemplo, si se usa un dispositivo de control destructivo, como un postquemador, un incinerador o una unidad de oxidación catalítica en el escape, una parte de los COVs presentes en la corriente serán oxidados de modo que no es razonable suponer que las pérdidas de COVs en el proceso son equivalentes a las emisiones ya que una parte de ellas está siendo controlada por dispositivos de control de emisiones. En este caso, las características y cantidades de las emisiones de COVs deberán determinarse con base en otras técnicas de estimación de emisiones como factores de emisión o modelos.
También se pueden llevar a cabo balances de materiales para calcular las emisiones fugitivas de fuentes de área que incluyan la producción, distribución y consumo de combustibles. Por ejemplo, en un estudio enfocado a determinar este tipo de emisiones en EU se aplicó un balance de materiales para la distribución y consumo de combustibles (De Luchi, 1993). Un balance de materiales a nivel nacional para solventes en pinturas podría ser también el mejor método para estimar las emisiones de COVs de esta categoría de fuentes. Un enfoque similar puede adoptarse para estimar las emisiones a la atmósfera derivadas de la aplicación de plaguicidas. Sin embargo, existen ciertas excepciones donde hay consideraciones adicionales que es necesario tener en cuenta. Por ejemplo, las emisiones del desengrasado no son iguales al consumo de solvente si el solvente residual es vendido a un reciclador comercial. En esta situación las emisiones serán la diferencia entre el solvente consumido y el solvente enviado a reprocesamiento. En un ejemplo más, se cree que alguna fracción del diluyente usado para licuar asfalto rebajado es retenida en el pavimento y no se evapora después de la aplicación.
El ejemplo siguiente muestra que, en algunos casos, la suposición de que todo el solvente consumido es equivalente a las emisiones de COV del proceso, resultaría en una sobrestimación de las emisiones. Por lo tanto, se utilizan balances de materiales junto con factores de emisión basados en el proceso para estimar las emisiones. Estos balances son parecidos a aquellos que se basan en la diferencia entre la materia prima y el producto, cuando el factor de emisión para un proceso está dado por unidad de material consumido.
Calcular las emisiones mensuales de COVs de un desengrasador de vapor. Cada mes, se añaden 100 litros de solvente al inicio del mes. A principios de mes, se añaden otros 20 litros para rellenar las pérdidas. A fin de mes, se envían 100 litros de solvente residual a un reciclador y 0.2 kg de residuos sólidos son recolectados para disposición.
El solvente es 100% COVs.
El solvente residual es 98% COVs.
El residuo sólido es 5% COVs.
La densidad del solvente es de 1.5 kg/litro.
Qsolvente = (100 litros/mes + 20 litros/mes) x 1.5 kg/litro
= 180 kg/mes
Qresidual = (100 litros/mes x 1.5 kg/litro x 98% COV) + (0.2 kg/mes x 5% COV)
= 147 kg/mes + 0.01 kg/mes
= 147 kg/mes
ECOV = Qsolvente – Qresidual
= 180 – 147
= 33 kg/mes
Hay otras situaciones que pueden complicar el balance de materiales. En primer lugar, no todas las pérdidas de solventes de ciertas operaciones como el lavado en seco o el desengrasado, se dan en el sitio de la planta. En cambio, se pueden evaporar cantidades significativas de solventes en el sitio de disposición del solvente residual, a menos que sea incinerado o dispuesto de manera que se impida su evaporación posterior a la atmósfera. En general, se puede suponer que gran parte del solvente enviado a sitios de disposición se evaporará, sin embargo, se debe determinar si una parte del solvente asociado con varias operaciones se evapora en el punto de disposición más que en el punto de uso, ya que estas pérdidas pueden presentarse fuera del área cubierta por el inventario.
De la misma manera, en algunos procesos de evaporación no es posible emplear balances de materiales, debido a que la cantidad de material perdido es demasiado pequeña para ser determinada con exactitud usando los procedimientos de medición convencionales. Por ejemplo, la aplicación de balances de materiales a los tanques de almacenamiento de productos del petróleo por lo general no es factible, debido a que las pérdidas por respiración y por operación son demasiado pequeñas con respecto a la capacidad total promedio del tanque. En estos casos, es preferible aplicar técnicas de estimación de emisiones basadas en factores de emisión o en modelos.
En resumen, con excepción de algunos tipos de fuente tales como los ejemplos de uso de combustibles y de solventes presentados anteriormente, el balance de materiales debe ser utilizado como un método de «arriba hacia abajo» para evaluar qué tan razonables son las estimaciones de emisión generadas al usar otras técnicas, más que como el principal método de estimación.
3.1.2 Diseño de Procesos
3.1.2.1 Destilación de compuestos orgánicos
Xileno, estireno, tolueno y benceno están siendo separados con el arreglo de columnas de destilación que se muestran a continuación donde F, D, B, D1, B1, D2 y B2 son los flujos molares en mol/min.
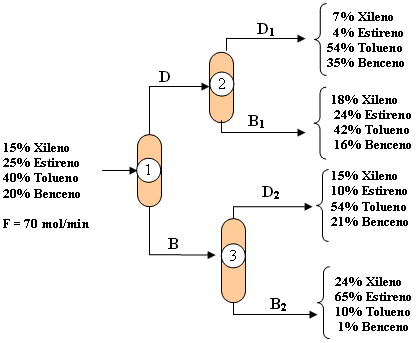
Figura 3. 1 Tren de separación
Los balances de materiales para componentes individuales sobre todo el tren de separación da el siguiente conjunto de ecuaciones
Xileno: 0.07D1+0.18B1+0.15D2 + 0.24B2 = 0.15 x 70
Estireno: 0.04D1+0.24B1+0.10D2 + 0.65B2 = 0.25 x 70
Tolueno: 0.54D1+0.42B1+0.54D2 + 0.10B2 = 0.40 x 70
Benceno: 0.35D1+0.16B1+0.21D2 + 0.01B2 = 0.20 x 70
En notación matricial, el sistema anterior se escribe:
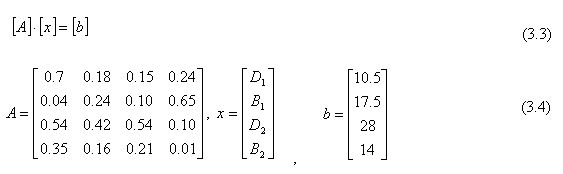
1. Aplicando MATLAB, para resolver el sistema de la Ecuación. 3.4, hacemos lo siguiente:
1.1 Escribimos la matriz A y el vector b
>> A= [0.07 0.18 0.15 0.24; 0.04 0.24 0.10 0.65; 0.54 0.42 0.54 0.10; 0.35 0.16 0.21 0.01]
A =
0.0700 0.1800 0.1500 0.2400
0.0400 0.2400 0.1000 0.6500
0.5400 0.4200 0.5400 0.1000
0.3500 0.1600 0.2100 0.0100
>> b=[10.5; 17.5; 28; 14]
b =
10.5000
17.5000
28.0000
14.0000
1.2 Damos la orden para calcular x:
x =
26.2500
17.5000 Flujos totales de salida de las
8.7500 Columnas 2 y 3
17.5000
>>
Balance total y de componentes individuales en la columna #2 pueden ser usados para determinar el flujo molar y fracciones molares a partir de la ecuación de la corriente D por:
Flujos molares: D = D1 + B1
Xileno : XDxD = 0.07D1 + 0.18B1
Estireno: XDsD = 0.04D1 + 0.24B1
Tolueno: XDtD = 0.54D1 + 0.42B1
Benceno: XDbD = 0.35D1 + 0.16B1
donde XDx = fracción molar de Xileno, XDs = fracción molar de Estireno, XDt = fracción molar de Tolueno, y XDb= fracción molar de Benceno.
De manera similar, balances total y de componentes individuales en la columna #3 pueden ser usados para determinar el flujo molar y las fracciones molares de la corriente B a partir del conjunto de ecuaciones:
Flujos Molares: B = D2 + B2
Xileno: XBxB = 0.15D2 + 0.24B2
Estireno: XBsB = 0.10D2 + 0.65B2
Tolueno: XBtB = 0.54D2 + 0.10B2
Benceno: XBbB = 0.21D2 + 0.01B2
Reemplazando los demás valores se tiene la solución completa.
3.1.3 Proceso de tratamiento de metales
Las superficies de metal son a menudo limpiadas usando solventes orgánicos en un tanque desengrasador abierto por el tope. Uno de los solventes ampliamente usados para tales operaciones es 1,1,1 – tricloroetano (TCE). El TCE pertenece a un grupo de productos químicos altamente estables conocido como agotadores de ozono. La Figura 3.2 bosqueja una operación típica que desengrasa. El factor de emisión para el proceso mostrado es estimado a ser 0.6 lb/lb de TCE entrando en el desengrasador.
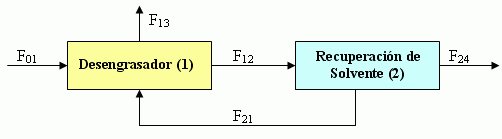
Figura 3.2. Esquema de una operación típica de desengrasado.
El solvente del desengrasador es enviado a una unidad de recuperación de solvente donde 80 % del solvente es recobrado y 20 % del solvente es evacuado con el lodo.
1. Para averiguar la viabilidad de la instalación de un sistema de recuperación de vapor, determinar la cantidad de TCE enviado a la atmósfera por la libra de TCE nuevo usado.
2. Si el sistema de recuperación de vapor es 90 % eficiente, determine la fracción de tricloroetano perdido a la atmósfera y la fracción yendo con el lodo.
Solución
Asumiendo una base de 1 lb para F01.
Las ecuaciones de balance de masa alrededor de las dos unidades para el proceso sin la unidad de recuperación de vapor es:
1 + F21 = F12 + F13 (1)
F12 = F21 + F24 (2)
La Ecuación para la cantidad de emisiones de TCET en términos de la cantidad de TCE entrando al desengrasador es:
F13 = 0.6 ( 1 + F21 ) (3)
En adición, la cantidad de TCE recuperado en términos de la cantidad de solvente entrante a la unidad de recuperación es
F21 = 0.8F12 (4)
Tomando las Ecs (1), (3) y (4) se tiene el sistema:
F12 + F13 – F21 = 1 (1)
F13 – 0.6 F21 = 0.6 (3)
0.8F12 – F21 = 0 (4)
En notación matricial, el sistema anterior se escribe:
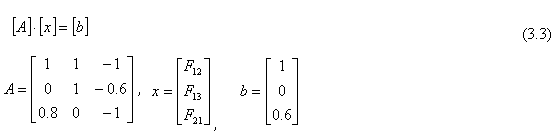
Con lo cual se tiene:
F12 = 0.5882 lbs
F13 = 0.8824 lbs
F21 = 0.476 lbs
Además:
F24 = 0.2 (F12) = 0.2* 0.5882 = 0.1176 lbs
b) Efectuar los cálculos cuando se adiciona una unidad de recuperación de vapor.
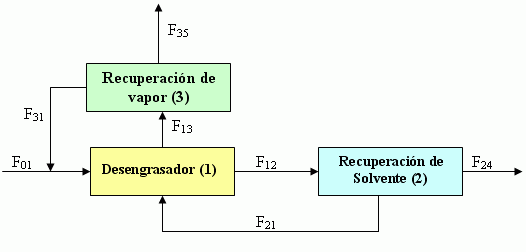
Figura 3.3. Esquema de la operación de desengrasado con una unidad de recuperación de vapor
